Nizozemski naučnici objavili su ovih dana da su vrlo blizu stvaranja prvih potpuno umjetnih organizama koji bi trebali biti efikasniji od prirodnih. Kako se život razvijao na Zemlji, svaki se novi korak nadograđivao na prethodni, što je dovelo do sve složenijih, ali ponekad i neefikasnih sistema.
Dobar primjer koji ilustrira koliko neefikasna mogu biti neka rješenja u prirodi je povratni grkljanski živac žirafe. Taj živac ide od mozga prema grlu, koje je njegov konačni cilj. Međutim, on kod žirafe, ali i kod drugih kičmenjaka, prolazi pored grla, spušta se sve do srca, gdje zaobilazi aortu, i vraća se nazad prema grkljanu.
Ova “obilazna ruta” imala je smisla kod životinja kratkih vratova, poput riba, kod kojih je živac kratkom putanjom povezivao mozak s najbližom strukturom škrga koja je kontrolisala osnovne funkcije disanja i gutanja. No ona je kod žirafe ekstremno neefikasna jer živac prelazi put od nekoliko metara umjesto da ide izravno do grla koje je kod žirafe od glave udaljeno svega desetak centimetara. Razlog za ovakav dizajn leži u evolucijskoj nadogradnji: promjene su se događale postupno, bez mogućnosti “redizajniranja” putanje živca koji je bio položen tako da ide oko aorte. To je rezultiralo nepotrebno dugim putem živca kroz vrat žirafe.
Inteligentno dizajniranje života od početka
Taj primjer jedan je od brojnih koji jasno pokazuju da dizajn živih bića nije stvorio inteligentni dizajner, već priroda kroz brojne evolucijske korake. No, u slučaju stvaranja života od početka, inteligentnim dizajnerskim rješenjima takve je neekonomičnosti moguće izbjeći.
Upravo to nastoji učiniti BaSyc (Building a Synthetic Cell), konzorcij od šest istraživačkih instituta koji radi na usavršavanju prirodnih procesa koji bi trebali dovesti do stvaranja umjetnog života. U dva nova rada tim BaSyca predstavio je značajne nove korake koji vode ka tom cilju.
Stvaranje sintetičkog života
Od 2017. godine BaSyc radi na stvaranju sintetičke ćelije, osnovne građevne jedinice života. Projekat se finansira kroz Grant Gravity nizozemskog Ministarstva obrazovanja, kulture i nauke te podršku Nizozemske organizacije za naučna istraživanja (NWO) koji su zajedno osigurali 18.8 miliona eura za početak istraživanja. Procjenjuje se da su preostale još dvije do tri godine do završetka ovog projekta.
“Konačni cilj projekta je konstruisati umjetne sisteme slične životu, koji mogu samostalno rasti, dijeliti se i održavati se. Razlikovaće se od poznatih živih ćelija, ali će imati iste ključne karakteristike”, rekao je u e-mailu za The Debrief vođa tima dr. Bert Poolman, profesor biohemije na Univerziteti u Groningenu.
Rješenje za energiju umjetnih ćelija
U jednom od svojih istraživanja, objavljenom 12. septembra 2024. u časopisu Nature Communications, tim BaSyca pokušao je riješiti problem opskrbe ćelije energijom. U prirodnim živim ćelijama, energiju potrebnu za njihovo funkcionisanje stvaraju mitohondrije (slika dolje) koji su dio energetskog sistema koji čine stotine različitih elemenata.

Tim BaSyca uspio je pojednostaviti taj prirodni dizajn tako što ga je u umjetnom sistemu sveo na samo pet elemenata. Prednost koju u razvoju umjetnih ćelija imaju naučnici sastoji se u tome da oni unaprijed dobro znaju prema kojem cilju dizajn sistema ide. To im omogućava da razviju najekonomičnija rješenja na najosnovnijoj razini, za razliku od evolucije, koja može samo nadograđivati ono što je već stvoreno, bez mogućnosti vraćanja unazad i preispitivanja ranijih odluka.
Postojeći mitohondriji funkcionišu kroz ciklus pretvaranja molekula ADP (adenozin difosfat) u ATP (adenozin trifosfat) i nazad, pri čemu se oslobađa energija potrebna za funkcionisanje ćelija. Sistem je smješten u male ćelijske vrećice, vezikule. Prva vezikula u ciklusu kroz stanične stijenke apsorbira ADP i aminokiselinu arginin. ADP i arginin zajedno učestvuju u proizvodnji ATP-a, ključne molekule za pohranu energije. U tom procesu, ADP i arginin ulaze u reakciju u ćelijskoj mitohondrijskoj strukturi. Arginin se razlaže i oslobađa energiju koja omogućava dodavanje fosfatne skupine na ADP, pri čemu nastaje ATP.
Proces korištenja pohranjene energije je suprotan. ATP se razgrađuje nazad u ADP, pri čemu se odvaja jedna fosfatna grupa i oslobađa se pohranjena energija. Ova energija pokreće vitalne ćelijske procese poput rasta, diobe i transporta, dok se ADP može ponovo koristiti u ciklusu stvaranja energije.
Nedostatak svođenja mnoštva elemenata mitohondrijskog sistema na samo pet u umjetnim ćelijama je taj što sistem može raditi samo na argininu, a ne na mastima, šećerima ili na aminokiselinama koje uobičajeno mogu napajati stanice.
Jedinica za stvaranje naboja
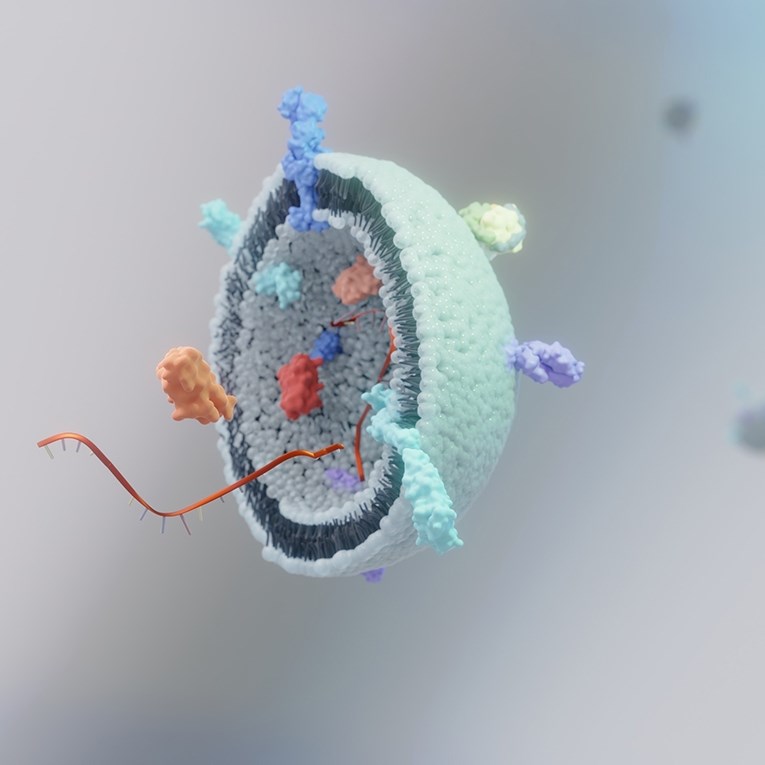
U drugom radu objavljenom 21. oktobra 2024. u časopisu Nature Communications tim je predstavio dizajn umjetne vezikule (slika dolje) koja može stvarati negativan električni naboj važan za transport i kompartmentalizaciju ADP-a i ATP-a.
Umjetna vezikula koristi hemijski proces u kojem pozitivno nabijeni proteini ulaze u nju i guraju druge molekule poput laktoze prema negativnom središtu, čime oponaša zbivanja u živim stanicama.
Testiranja su pokazala da umjetna vezikula može izvoditi složenije zadatke. Dodavanjem enzima uz laktozu, sistem je oksidirao šećer laktozu i stvorio koenzim NADH.
Kretanje prema sintetičkom životu
Iako su Poolman i njegovi saradnici iz BaSyca postigli značajan napredak, potrebno je još dosta rada prije nego što sintetičke ćelije postanu stvarnost. No, kada BaSycov program završi u sljedećih nekoliko godina, posao će nastaviti njegov nasljednik koji je već pripremljen.
Naime, NWO je osigurao dodatnih 40 miliona eura istraživačkog granta za program EVOLF, “Evolving Life from Non-life”. “Još smo 10-ak godina udaljeni od takvog umjetnog sistema sličnog životu”, rekao je dr. Poolman.
“U međuvremenu, puno učimo o biološkim mehanizmima i otkrivamo iznenađujuća svojstva koja se pojavljuju kada se biološke komponente spoje. Svojstva koja nisu vidljiva u pojedinačnim komponentama i koja će biti teško otkriti u složenim živim ćelijama… To će nam otkriti nacrt života i sličnih sistema, što je nešto što trenutno nedostaje”, dodao je Poolman.
“Jedan od sljedećih koraka je integracija modula za generiranje protonske pokretačke sile (Nat Commun) s modulom za proizvodnju ATP-a (Nat Nanotech), koji će funkcionisati u smislu očuvanja metaboličke energije kao što to rade mitohondriji, ali na mnogo jednostavniji način”, kaže nizozemski naučnik.
Poolman kaže da njegov tim trenutno takođe radi na povezivanju modula koji omogućava proizvodnju ATP-a sintezom lipida, što omogućava širenje membrane, te dodaje da će ga, u saradnji s kolegama u Nizozemskoj i inostranstvu, uskoro integrisati s modulima za diobu ćelija i sintezu proteina.